IF=30.9!肠道菌群-抗性淀粉-MASLD!国际顶级期刊《Cell Metabolism》最新发文!
肠道菌群的个体差异介导了抗性淀粉对代谢功能障碍相关脂肪性肝病(MASLD) 的疗效
导 读
2025年11月20日,上海交通大学医学院、国家自然科学基金优秀青年基金获得者(2021)李华婷研究员 (通讯作者) 团队在国际顶级期刊《Cell Metabolism》(Q1,IF2024=30.9)发表题为“Interindividual variability in gut microbiome mediates the efficacy of resistant starch on MASLD”的最新研究。李华婷研究员主要研究方向:糖尿病发病机制与诊疗新靶点,糖尿病基座人工智能模型研究,人工智能诊疗新技术研究。
本研究聚焦于代谢功能障碍相关脂肪性肝病(MASLD,原称 NAFLD),这一从单纯性脂肪变性到 MASH 并可进一步进展为纤维化、肝硬化乃至肝癌的全球性健康危机。尽管其致病机制复杂,但目前仅有 resmetirom 一种药物获批用于 MASH,亟需新的干预策略。在多种候选方案中,益生元因其调控肠道菌群的潜力而备受关注。研究团队此前的临床试验显示,具有益生元特性的抗性淀粉(RS)可显著改善 MASLD:肝内甘油三酯减少约 39%,肝酶与血脂指标亦同步改善。这些效应依赖于RS 对肠道菌群的重塑,包括提升有益菌丰度、降低潜在致病菌等。
然而,越来越多证据表明,个体对益生元干预的反应存在显著差异,且这种差异往往超过所使用的益生元类型本身。这种异质性限制了干预效果,也阻碍了个性化治疗的发展,因此理解其机制对于实现患者分层和精准干预至关重要。MASLD 干预反应的差异可能源于遗传、表观遗传、菌群和生活方式等多重因素,其中肠道菌群被认为是调控代谢健康的关键决定因素。既往研究已发现 MASLD 不同阶段患者普遍存在菌群结构或功能的特异性改变。
在此背景下,本研究通过整合全景式多组学数据和统计分析,系统探索了基线肠道菌群如何驱动个体化的 RS 响应机制。研究进一步通过随访试验、人源关键菌株的分离,以及体内外实验加以验证。基于核心微生物特征构建的 XGBoost 预测模型显示出良好的预测能力,为未来开展个性化的 MASLD 干预提供了可行框架与理论基础。
成果介绍
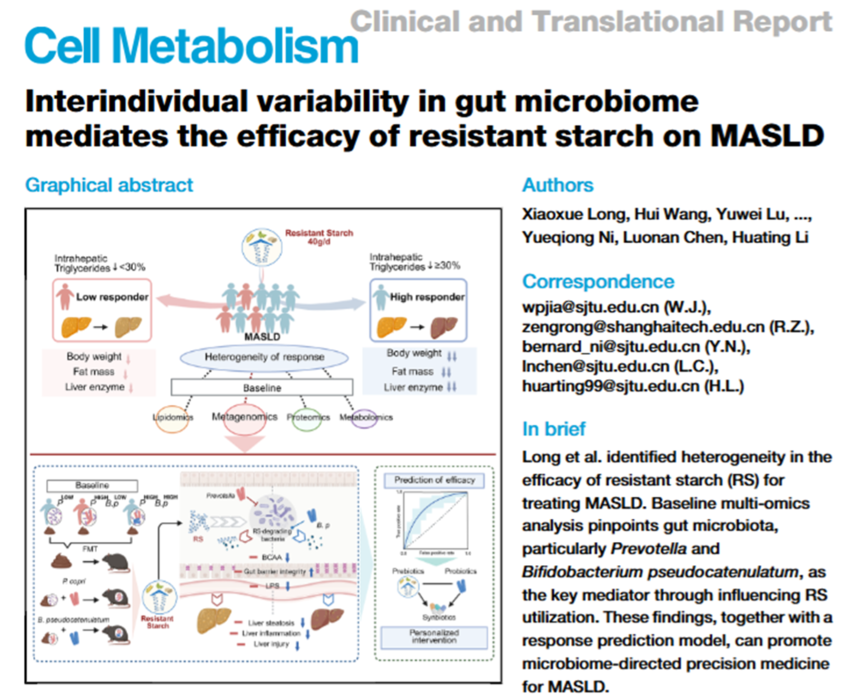
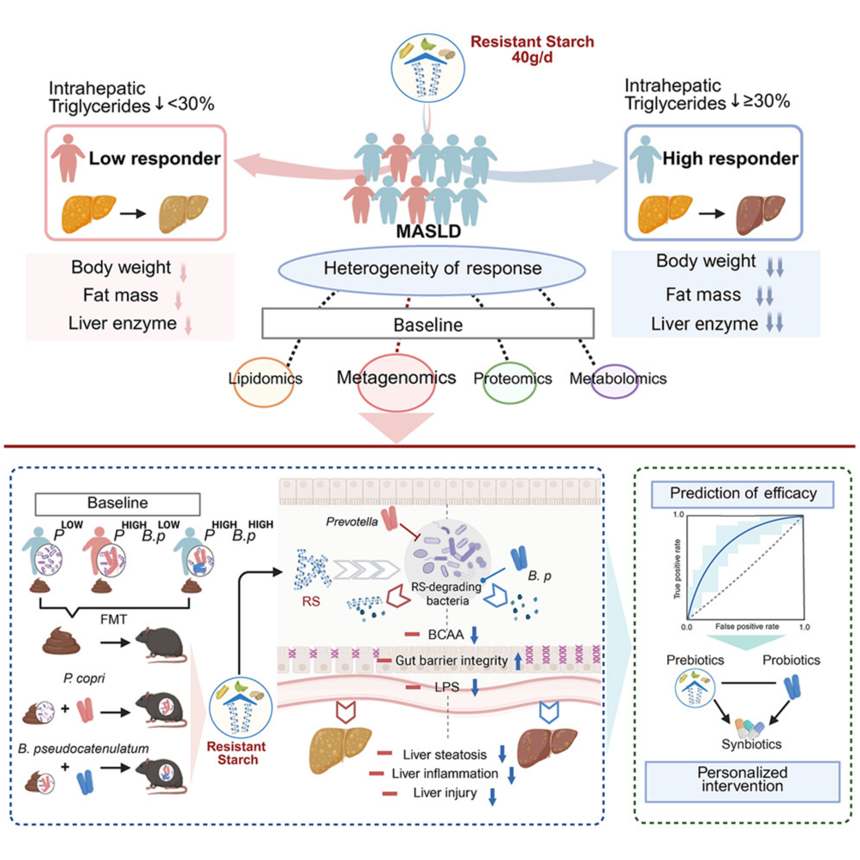
该研究团队在一项随机、安慰剂对照试验中发现,抗性淀粉(RS)作为一种益生元,对代谢功能障碍相关脂肪性肝病(MASLD)具有治疗作用。本研究中,我们观察到其疗效存在异质性,其中约30%的参与者获益有限,这一现象在另一项多中心试验(ChiCTR2300074588)中得到了重复验证。多组学分析与粪菌移植实验表明,基线肠道菌群是影响干预反应的主要因素。进一步的人群分层和网络分析结合体外与体内实验揭示,普雷沃氏菌属(Prevotella)是导致低反应的关键原因,它通过抑制 RS 降解菌从而削弱 RS 的利用。相反,我们从队列中分离得到的双歧杆菌 Bifidobacterium pseudocatenulatum RRP01 能恢复 RS 的降解,并改善被 Prevotella 削弱的 RS 反应。 此外,该研究团队还开发了一个整合基线微生物和临床特征的预测模型(曲线下面积 AUC = 0.74–0.87),可用于实现个性化干预的人群分层。研究结果表明,肠道菌群决定了 RS 疗效的异质性,并为开发面向 MASLD 的微生物精准治疗提供了新可能。
图文赏析
“版权归原作者平台所有,如有侵权请联系删除,谢谢”!
推荐
-

-

QQ空间
-

新浪微博
-

人人网
-

豆瓣




